南京中國eCTD系統
eCTD提交流程與ESG系統:FDA要求通過電子提交網關(ESG)傳輸eCTD文件,單個文件大小限制為10GB,超限需拆分或通過物理介質(如光盤)遞交。提交前需預分配申請號(如NDA編號),并通過ESG測試賬戶驗證技術合規性。序列號命名規則為4位數字(如0001),申請需從“原申請”序列開始,補充資料按遞增順序編號。企業可自愿提交預審樣本(Pre-Submission),FDA將反饋文檔結構、元數據等合規性問題。驗證標準與常見錯誤類型:FDA驗證標準分為高(High)、中(Medium)、低(Low)三級,高風險錯誤(如無效XML或缺失關鍵表格)必須修復,否則直接拒收。常見問題包括:重復序列號(錯誤1034)、文件路徑超長(警告2015)、PDF加密或非標字體(錯誤4001)。2023年統計顯示,30%的提交因模塊1格式錯誤被退回,凸顯行政信息合規的重要性。驗證工具如LORENZ eValidator被FDA官方采用,可自動檢測200+項技術指標。澳大利亞eCTD注冊外包相關技術支持。南京中國eCTD系統

eCTD即是電子化的CTD注冊申報方式,相對于傳統的紙質遞交,eCTD電子遞交更便捷、更安全。對于申請者來說,一個產品如在多個市場遞交,M2-M5的資料可以共享,極大降低了成本并提高了效率;對審評者來說,eCTD資料的審閱、管理、傳輸以及歸檔十分便捷,eCTD格式同時也利于各個地區的yao監部門的審評意見交流。eCTD遞交自2003年開始實施以來,以其在創建、傳輸、復制、審閱、檢索、存檔以及文件生命周期管理等方面的優勢當之無愧地成為全球YAO品注冊申報的大勢所趨,除了傳統的美國、日本和歐盟等ICH成員國之外,加拿大、瑞士、沙特阿拉伯、南非、澳大利亞、新西蘭、泰國、新加坡、韓國等地區都已經部分采納或者正在逐步轉向eCTD遞交。賦悅科技,做為國內自主研發服務器版eCTDYAO品注冊申報軟件,讓法規注冊事務從系統上極大縮短申報周期,助力企業加快產品上市速度。迅速實施,上手簡單,項目管理,超鏈接管理,權限管理,審計追蹤;網頁登錄,異地辦公,多人協同,eCTD文件導入,PDF批量一鍵修復。同時提供短期租賃服務,在保證合規的前提下,為企業降本增效。 徐匯區國際注冊eCTD軟件中ANDA注冊申報相關技術支持。
法規文檔管理系統 協同共享 RDMS可以讓跨區域、跨部門協同真正成為1+1>2的 工作。讓頻繁的文檔共享傳輸,版本管理,生命周 期審批都變得輕松簡單 安全合規 通過詳細的審計追蹤、電子簽名、權限管理、網 關控制、頁面控制等技術手段,構建安全合規的 文檔管理系統,通過安全驗證與合規驗證 統一文檔來源 藥品注冊是企業經營成果的技術資料,由多個部門 長時間匯集到法規部門。RDMS確保多部門文檔來 源統一,即使人員流動也可以快速接續工作 統一文檔結構 根據不同申報類型,自動生成文檔結構,讓法規 人員與跨部門同事掌握申報需要的資料需求,降 低溝通成本,降低經驗需求,避免疏忽遺漏
PDF工具箱批量處理與格式修復支持PDF合并、拆分、提取頁面、旋轉頁面等操作,可批量修復字體未嵌入、超鏈接錯誤等問題,確保文件符合注冊法規要求。智能書簽與超鏈接管理提供書簽導入/導出、超鏈接自動生成(支持關鍵字搜索鏈接)、題注超鏈接拖拽式編輯等功能,簡化復雜文檔的導航設計。文檔轉換與OCR識別支持Word轉PDF(自動生成書簽、嵌入字體),以及PDF與Word、Excel等格式互轉,集成OCR功能用于掃描件文字識別。合規性驗證自動驗證PDF的頁面布局、頁碼連續性、空白頁、目錄層級等屬性,并具體錯誤位置,減少人工檢查成本。安全與協作功能支持文檔加密、數字簽名、云端同步及多設備共享,滿足企業級文件安全管理需求。瑞士eCTD注冊外包相關技術支持。
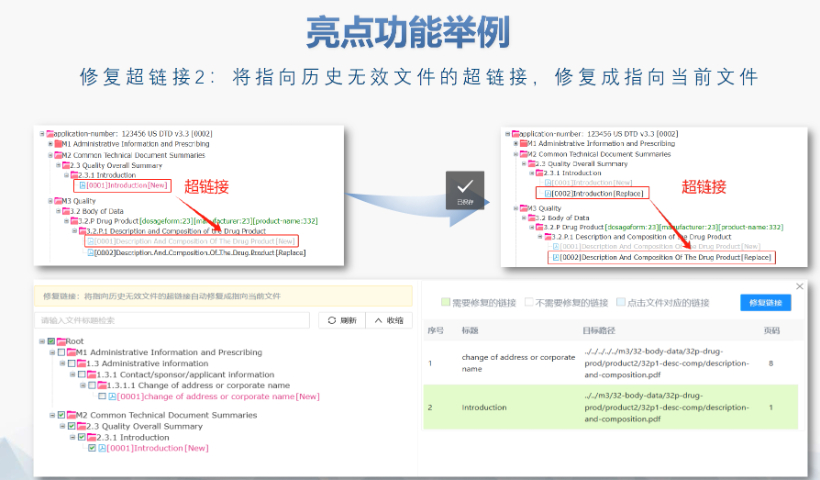
文件生命周期管理:eCTD支持文件替換(Replace)、刪除(Delete)等操作,而非增文件。例如,更臨床研究方案時需用Replace操作覆蓋舊版本。基線提交(BaselineSubmission)可用于補充歷史紙質資料,但需在封面函中聲明無內容變更。臨床數據與研究標簽文件(STF):模塊4和5中的研究數據需通過STF(StudyTaggingFiles)引用,確保數據與文檔關聯。FDA要求數據集(如SASXPORT格式)能置于模塊3-5,且單個文件超過4GB需拆分。2022年統計顯示,58%的ANDA因研究數據技術拒絕標準(TRC)錯誤被拒。電子簽名與表格要求:FDA表格(如356h、1571)需使用數字簽名,PDF文件禁止加密或設置編輯限制。電子簽名需符合21CFRPart11規范,確保身份驗證、不可否認性和數據完整性。外包服務與系統解決方案:賦悅科技累計提交超2000份eCTD申請,外包可降低40%人工錯誤率。歐盟NDA注冊申報相關技術支持。青海國際注冊eCTD
瑞士IND注冊申報相關技術支持。南京中國eCTD系統
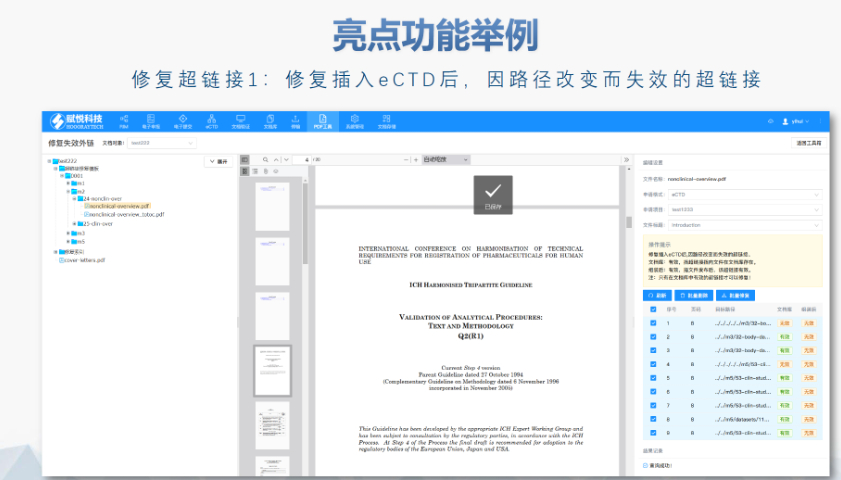
美國eCTD驗證采用三級分類:“錯誤”(必須修正)、“警告”(建議修正)、“提示信息”(參考)。例如,PDF文件版本不符或加密保護屬于“錯誤”,而書簽路徑非相對性則可能列為“警告”。驗證失敗將直接導致退審,企業需通過LORENZ Validator等工具預檢,確保提交前合規。 ?技術驗證點 驗證涵蓋XML結構合規性、文件命名規則、生命周期管理(如序列號連續性)及PDF屬性(如字體嵌入、可搜索性)。臨床試驗數據需額外滿足CDISC標準,包括SDTM和ADaM數據集的結構驗證南京中國eCTD系統
- 黑龍江化學藥品eCTD 2025-07-16
- 工業園區化學藥品eCTD名稱 2025-07-16
- 南京中國eCTD系統 2025-07-16
- 高新區中國eCTD歡迎選購 2025-05-14
- 靜安區生物制品eCTD使用 2025-05-14
- 蕪湖新藥eCTD是什么 2025-05-14
- 吳江區賦悅科技eCTD供應商 2025-05-14
- 南京生物制品eCTD注冊系統 2025-05-14
- 上海化學藥品eCTD格式 2025-05-09
- 南京電子申報eCTD哪個品牌好 2025-05-09
- 吉林移動端設備管理系統軟件 2025-07-21
- 湖州跨境供應鏈外貿軟件 2025-07-21
- 南京定制服務企來搭企業AI數字化轉型軟件 2025-07-21
- 湛江星光級攝像頭模組找哪家 2025-07-21
- 柳州水力無人機巡檢方案 2025-07-21
- 佛山usb攝像頭什么價格 2025-07-21
- 數字孿生與CIM平臺特點 2025-07-21
- 上海推薦企來搭數字化AI轉型 2025-07-21
- 浦東新區小程序開發哪家強 2025-07-21
- 前端小模型邊緣計算生態 2025-07-21