北京外泌體提取試劑進(jìn)貨價(jià)
外泌體在肺病進(jìn)程中的作用:在一些病癥微環(huán)境中,一些病癥細(xì)胞來(lái)源的外泌體能夠誘導(dǎo)CD4+T分化為調(diào)節(jié)性T細(xì)胞,壓制機(jī)體的抗一些病癥免疫反應(yīng);肺病細(xì)胞分泌的外泌體含有miR-21和miR-29a,可在免疫細(xì)胞中結(jié)合并啟動(dòng)TLR8,使TLR介導(dǎo)的NF-κB信號(hào)通路活化,從而導(dǎo)致一些病癥的生長(zhǎng)和轉(zhuǎn)移。在肺病的侵襲和轉(zhuǎn)移過(guò)程中,細(xì)胞間通訊扮演著重要的角色。據(jù)有關(guān)報(bào)道稱(chēng),NSCLC分泌的外泌體內(nèi)TGFβ和IL10的高表達(dá)與肺病的轉(zhuǎn)移密切相關(guān)。此外,啟動(dòng)的T細(xì)胞可以通過(guò)調(diào)控Fas信號(hào)通路增加基質(zhì)金屬蛋白酶9(MMP9)的表達(dá),進(jìn)而促進(jìn)肺病的轉(zhuǎn)移。這些機(jī)制有望成為肺病治病的潛在靶點(diǎn)。雖然大多數(shù)外泌體都是促進(jìn)一些病癥的侵襲與轉(zhuǎn)移,但也有報(bào)道稱(chēng),外泌體miR-302b可以通過(guò)壓制TGFβRⅡ來(lái)壓制肺病細(xì)胞的轉(zhuǎn)移與增殖。如純度和回收率低,雜蛋白較多(假陽(yáng)性),顆粒大小不均一,產(chǎn)生難以去除的聚合物。外泌體目前被視為特異性分泌的膜泡,參與細(xì)胞間通訊。北京外泌體提取試劑進(jìn)貨價(jià)
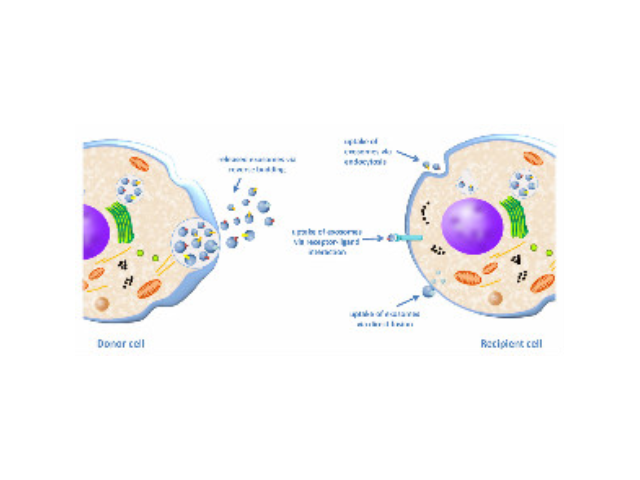
研究初次發(fā)現(xiàn)瘧原蟲(chóng)傳染小鼠血漿外泌體(exosomes)能夠壓制一些病癥血管生成,并初步闡明其分子機(jī)制。研究加深了對(duì)瘧原蟲(chóng)傳染宿主所分泌的外泌體與一些病癥血管生成之間的相互作用的認(rèn)識(shí),為開(kāi)發(fā)瘧原蟲(chóng)傳染來(lái)源的外泌體作為一種新型抗一些病癥制劑奠定了基礎(chǔ)。研究人員選用肺病小鼠模型作為研究對(duì)象,從傳染瘧原蟲(chóng)的小鼠血漿中獲得外泌體,并將這些外泌體注射到小鼠的一些病癥內(nèi)部,并與沒(méi)有瘧原蟲(chóng)傳染的小鼠血漿外泌體進(jìn)行對(duì)照。研究發(fā)現(xiàn),瘧原蟲(chóng)傳染小鼠的血漿外泌體明顯壓制一些病癥血管的生成。進(jìn)一步的研究發(fā)現(xiàn),瘧原蟲(chóng)傳染的小鼠血漿外泌體通過(guò)至少四種特殊的微小RNA(miR16-5p/17-5p/322-5p/497-5p)壓制血管內(nèi)皮細(xì)胞VEGF受體(VEGFR2)的表達(dá)從而阻斷血管生成的信號(hào)通路。這些發(fā)現(xiàn)加深了人們對(duì)瘧原蟲(chóng)抗病機(jī)理的理解,并為瘧原蟲(chóng)療法治病一些疾病的臨床研究提供進(jìn)一步的理論依據(jù)。廣州正規(guī)外泌體提取試劑產(chǎn)品介紹外泌體提純?cè)噭┖械奶厣c優(yōu)勢(shì):無(wú)需沉淀試劑,也無(wú)需過(guò)夜培養(yǎng)。

外泌體(exosome)是所有細(xì)胞釋放出的菌類(lèi)大小的顆粒。它們天然地存在于血液中。根據(jù)來(lái)自美國(guó)德州大學(xué)MD安德森一些疾病中心的一項(xiàng)新的研究,對(duì)外泌體進(jìn)行基因操縱可能提供一種新的胰腺病治病方法。論文通信作者為德州大學(xué)MD安德森一些疾病中心一些疾病生物學(xué)系研究員RaghuKalluri博士。在這項(xiàng)新的研究中,經(jīng)過(guò)基因修飾的外泌體(被稱(chēng)作iExosome)能夠運(yùn)送特異性地靶向KRAS突變基因的小RNA分子,從而導(dǎo)致胰腺病模式小鼠病情緩解,增加它們的總存活率。這些研究人員采用了一種被稱(chēng)作RNA干擾(RNAi)的靶向方法:利用這些天然的納米顆粒(即外泌體)運(yùn)送小干擾RNA(siRNA)或短發(fā)夾RNA(shRNA)分子來(lái)靶向胰腺病細(xì)胞中的KRAS突變基因,從而影響多種胰腺病模型的一些病癥負(fù)荷和存活。他們證實(shí)外泌體能夠作為一種高效的RNAi載體發(fā)揮作用,這是因?yàn)檫@些納米大小的囊泡(即外泌體)輕松地在體內(nèi)遷移和進(jìn)入靶細(xì)胞(包括病細(xì)胞)中。外泌體在免疫中抗原呈遞、一些病癥的生長(zhǎng)與遷移、組織損傷的修復(fù)等生理病理上起著重要的作用。
近年來(lái),隨著外泌體研究的不斷深入,它的應(yīng)用已經(jīng)涉及一些病癥治病領(lǐng)域、醫(yī)學(xué)基礎(chǔ)和免疫領(lǐng)域、寄生蟲(chóng)領(lǐng)域;臨床研究上已涉及心血管系統(tǒng)、內(nèi)分泌代謝系統(tǒng)等。外泌體來(lái)源及內(nèi)含物。幾乎所有類(lèi)型的細(xì)胞都可以分泌外泌體,同時(shí)外泌體也普遍存在于體液中,包括血液、眼淚、尿液、唾液、乳汁、腹水等。目前研究發(fā)現(xiàn)外泌體中富含核酸(microRNA、lncRNA、circRNA、mRNA、tRNA等)、蛋白、膽固醇等。外泌體的表面marker主要有CD63、CD81、CD9、TSG101、HSP27等。外泌體鑒定。目前對(duì)于外泌體的鑒定主要有四種方法:透射電子顯微鏡(TEM)、Nanosight、WesternBlot、流式細(xì)胞術(shù)。外泌體提取:超濾膜也可用于分離外泌體。
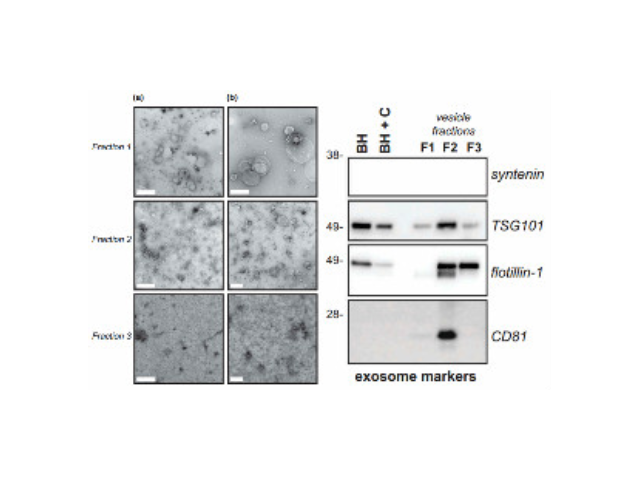
研究中研究人員發(fā)現(xiàn),胃病細(xì)胞周?chē)缓琓AM。TAM以M2極化表型為特征,并促進(jìn)胃病細(xì)胞在體外和體內(nèi)的遷移。此外,研究人員發(fā)現(xiàn)M2衍生的外泌體決定了TAMs介導(dǎo)的遷移活動(dòng)。通過(guò)使用質(zhì)譜方法,研究人員確定載脂蛋白E(ApoE)是M2巨噬細(xì)胞衍生的外泌體中高度特異性和有效的蛋白質(zhì)。ApoE是一種M2特異性且高度豐富的來(lái)源于M2外泌體的蛋白質(zhì),是決定胃病細(xì)胞遷移潛力的主要驅(qū)動(dòng)因素。然而,來(lái)自ApoE-/-的小鼠M2巨噬細(xì)胞的外泌體在體外和體內(nèi)對(duì)胃病細(xì)胞的遷移沒(méi)有顯著影響。在機(jī)制上,M2巨噬細(xì)胞衍生的外泌體介導(dǎo)ApoE啟動(dòng)的PI3K-Akt信號(hào)通路,并在TAM和受體胃病細(xì)胞之間進(jìn)行細(xì)胞間轉(zhuǎn)移,促進(jìn)細(xì)胞骨架的遷移。總的來(lái)說(shuō),該研究發(fā)現(xiàn)外泌體介導(dǎo)的功能性ApoE蛋白從TAM轉(zhuǎn)移到一些病癥細(xì)胞,促進(jìn)了胃病細(xì)胞的遷移。無(wú)法實(shí)現(xiàn)臨床的常規(guī)化應(yīng)用。昆明外泌體提取試劑價(jià)格
外泌體提取:具有高粘度的生物樣品。北京外泌體提取試劑進(jìn)貨價(jià)
2018版《指導(dǎo)要求》說(shuō)明外泌體沒(méi)有限定單一的分離手段,多種手段都可以進(jìn)行細(xì)胞外囊泡的富集。《指導(dǎo)要求》編寫(xiě)者們認(rèn)為“高回收率,低特異性”的富集手段是指那些富集囊泡的同時(shí)會(huì)有大量的非囊泡組分被富集,甚至細(xì)胞的整個(gè)分泌組都會(huì)被摻入其中,歸入這一類(lèi)的分離手段主要包括通過(guò)改變電荷或通過(guò)高聚物作用的沉淀試劑盒、低分子量截流的超濾分離、超長(zhǎng)時(shí)間和超高離心力的超速離心等。Wako的MagCapture?ExosomeIsolationKitPS(產(chǎn)品編號(hào)299-77603(2tests),293-77601(10tests)),使用PS親和法對(duì)外泌體進(jìn)行提取,損失小且能獲得高純度的外泌體。北京外泌體提取試劑進(jìn)貨價(jià)
- 正規(guī)外泌體提取試劑推薦廠(chǎng)家 2025-06-19
- 溫州細(xì)胞外基質(zhì)膠產(chǎn)品介紹 2025-06-18
- 合肥正規(guī)外泌體提取試劑廠(chǎng)家直銷(xiāo) 2025-06-18
- 濟(jì)南外泌體提取試劑廠(chǎng)家批發(fā)價(jià) 2025-06-18
- 金華正規(guī)細(xì)胞外基質(zhì)膠供應(yīng)商 2025-06-18
- 金華正規(guī)細(xì)胞外基質(zhì)膠廠(chǎng)家現(xiàn)貨 2025-06-18
- 濟(jì)南正規(guī)外泌體提取試劑廠(chǎng)家推薦 2025-06-18
- 南京正規(guī)外泌體提取試劑報(bào)價(jià) 2025-06-18
- 北京外泌體提取試劑服務(wù)電話(huà) 2025-06-18
- 深圳細(xì)胞外基質(zhì)膠哪里買(mǎi) 2025-06-18
- 興安盟酒店洗衣粉出口 2025-06-19
- 晉中布草洗滌定制生產(chǎn) 2025-06-19
- 梅州水浴鍋實(shí)驗(yàn)室設(shè)備 2025-06-19
- 山東UV膠價(jià)格 2025-06-19
- 貴陽(yáng)細(xì)胞外基質(zhì)膠銷(xiāo)售廠(chǎng)家 2025-06-19
- 貴州微乳化切削液 2025-06-19
- 浙江透明UV膠使用方法 2025-06-19
- 南通維生素k2粉末廠(chǎng)家 2025-06-19
- 華東GABA調(diào)制乳采購(gòu) 2025-06-19
- 正規(guī)外泌體提取試劑推薦廠(chǎng)家 2025-06-19