遼寧推薦的肺纖維化模型動物實驗外包
肺纖維化動物模型的建立方法主要分為生物因素及非生物因素2大類。②采用非生物因素誘導建立肺纖維化模型的方法雖然在產生肺纖維化程度上較為不穩定,但在藥物選擇和給藥途徑方面具有多樣性,且操作簡單,價格低廉,所以在造模方式的選擇上較為常見,非生物因素誘導建立的肺纖維化模型主要包括藥物/毒物因素(博來霉素、胺碘酮、油酸、***及異硫氰酸熒光素)、環境因素(二氧化硅、石棉及高濃度氧)和其他因素(人源化及老年化)誘導的模型構建建模方法。③生物因素誘導的肺纖維化模型,多見于選擇細胞因子過表達或靶向Ⅱ型肺泡上皮細胞損傷,這類模型與肺纖維化臨床后期表現更為相似,且模型穩定性好,但是價格較昂貴。科學家通過肺纖維化模型發現了一些與疾病相關的微小RNA。遼寧推薦的肺纖維化模型動物實驗外包
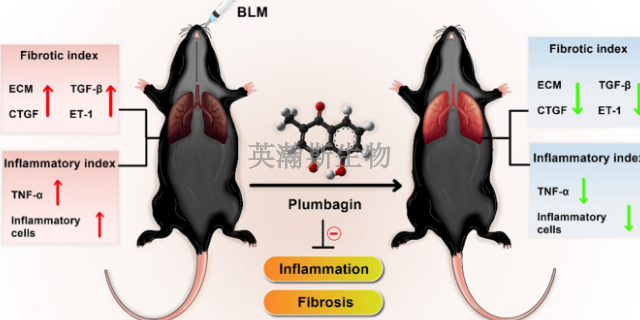
許多物質和疾病都可以導致肺纖維化。即便如此,在很多情況下無法找到具體原因。不明原因的肺纖維化叫做特發性肺纖維化。研究人員對引發特發性肺纖維化的原因有幾種理論,包括病毒和接觸***煙霧。此外,一些形式的特發性肺纖維化在家族中遺傳,遺傳可能在特發性肺纖維化中發揮作用。許多特發性肺纖維化患者也可能患有胃食管反流病(GERD)—一種胃酸流回食管的疾病。目前已有研究在評估GERD是否可能是導致特發性肺纖維化的風險因素,或者GERD是否可能導致病情進展更快。但還需要開展更多的研究來確定特發性肺纖維化與GERD之間的聯系。海南靠譜的肺纖維化模型有哪些肺纖維化模型為研究疾病過程中的微生物組變化提供了平臺。
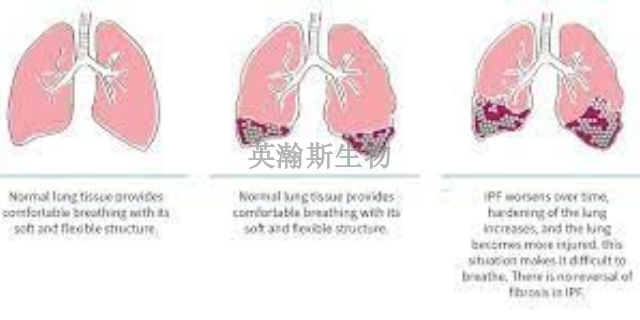
肺纖維化模型在肺纖維化研究領域中具有不可替代的地位,其中尤為突出的是它為研究肺纖維化的遺傳因素提供了極大的便利。遺傳因素在肺纖維化的發病過程中扮演著重要角色,不同的基因變異可能導致個體對肺纖維化的易感性增加。通過肺纖維化模型,研究人員能夠模擬不同基因背景下的肺纖維化過程,從而深入探討特定基因變異對疾病進程的影響。這種模型的應用使得研究人員能夠在實驗室中模擬出類似于人類的遺傳背景,進而研究遺傳因素在肺纖維化中的作用機制。這不僅有助于揭示肺纖維化的遺傳基礎,還為基于遺傳學的療愈策略的開發提供了重要的理論支持。
肺纖維化模型在肺纖維化疾病研究中扮演著重要角色,尤其是為研究疾病過程中的細胞凋亡和自噬提供了理想的實驗平臺。細胞凋亡和自噬是兩種重要的細胞自我調控機制,它們在維持細胞穩態和應對外界壓力中起著關鍵作用。在肺纖維化的過程中,這兩種機制可能會受到干擾,導致細胞死亡和細胞功能的異常。通過肺纖維化模型,研究人員能夠模擬出與肺纖維化相似的病理環境,觀察和分析細胞凋亡和自噬的變化。這不僅有助于我們更深入地理解肺纖維化的發病機制,還能為開發新的療愈策略提供科學依據。因此,肺纖維化模型為研究疾病過程中的細胞凋亡和自噬提供了寶貴的平臺。肺纖維化模型有助于評估不同藥物在肺纖維化療愈中的安全性。
科學家們通過使用肺纖維化模型,精心模擬了人類肺纖維化的復雜病理過程。這一模型高度還原了肺組織在炎癥、損傷和修復過程中的變化,包括炎癥細胞的浸潤、膠原蛋白的過度沉積以及肺組織結構的重構等關鍵步驟。通過這一模型,科學家們能夠深入觀察和研究肺纖維化的發生和發展機制,從而更準確地理解疾病的本質。這種模擬不僅有助于揭示肺纖維化的發病機理,也為科學家們提供了評估潛在療愈方法和藥物效果的平臺,為肺纖維化的預防和療愈提供了新的思路和方法。肺纖維化模型有助于評估肺纖維化療愈對患者生活質量的影響。海南靠譜的肺纖維化模型有哪些
在肺纖維化模型中,肺纖維化的進程與肺部微環境的改變密切相關。遼寧推薦的肺纖維化模型動物實驗外包
肺纖維化模型發展時間:給藥后第 7 天肺組織大多呈重度肺泡炎改變,肺泡腔及肺間質內有大量中性粒細胞浸潤,部分肺泡腔破壞或消失,肺間隔內成纖維細胞和***增生,與正常肺組織對比差別明顯;給藥后第14天,肺纖維化開始形成。巨噬細胞、中性粒細胞等炎性細胞明顯減少,成纖維細胞增多,肺泡間隔明顯增厚,有膠原沉積。給藥后第28天,多數小鼠發生彌漫性肺間質纖維化,肺間質被膠原纖維和成纖維細胞替代,肺泡壁破壞,肺大泡形成,但仍可見炎性細胞浸潤。遼寧推薦的肺纖維化模型動物實驗外包
- 遼寧推薦的肺纖維化模型動物實驗外包 2025-07-09
- 湖北大鼠肺纖維化模型動物實驗外包 2025-07-09
- 寧夏免疫組化檢測 2025-07-09
- 河南肺纖維化模型怎么造模 2025-07-09
- 河南靠譜免疫組化要多久 2025-07-09
- 青海肺纖維化模型有哪些 2025-07-09
- 甘肅大鼠免疫組化要多久 2025-07-09
- 廣東推薦的肺纖維化模型是哪家 2025-07-09
- 陜西專業的肺纖維化模型怎么造模 2025-07-09
- 江蘇真實的肺纖維化模型有哪家 2025-07-09
- 貴州高分子夾板效果 2025-07-09
- 徐州介紹智能健康管理系統戰略 2025-07-09
- 北京人工活動義眼生產 2025-07-09
- 靜安區內鏡洗消追溯系統廠家電話 2025-07-09
- 水浴滅菌生物指示劑大概價格 2025-07-09
- 貴陽福莫特羅中間體3-硝基-4-芐氧基-2-溴代苯乙酮 2025-07-09
- 成都一次性血液過濾器一站式環氧乙烷滅菌 2025-07-09
- 一次性血液過濾器EO滅菌公司哪家好 2025-07-09
- 浙江安全益生元是什么 2025-07-09
- 東北口腔水門汀代理商 2025-07-09